10/12/2024

La investigación, liderada por Lisette Leyton, destacó el papel de la vía de señalización PI3K/AKT, que juega un rol crucial en la activación de los astrocitos, las células del cerebro responsables de formar cicatrices en respuesta a un daño cerebral.
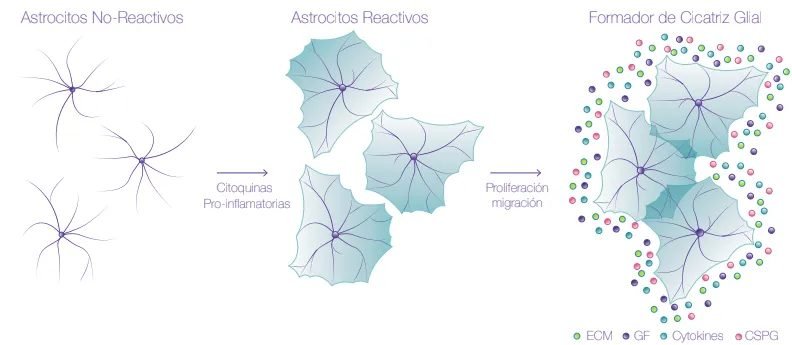
La gliosis es una reacción del cerebro a una lesión, en la cual las células gliales, como los astrocitos, se activan, se multiplican y cambian de forma para ayudar a reparar el daño. Estas células producen proteínas (citoquinas) que impulsan la inflamación para defenderse, pero, si esta respuesta es demasiado intensa o se prolonga por mucho tiempo, los astrocitos pueden volverse tóxicos para el cerebro, contribuyendo a una inflamación crónica que puede agravar el daño cerebral. Este fenómeno tiene un doble filo: por un lado, los astrocitos protegen al cerebro, pero si su reacción no es controlada, pueden acabar dañando las células nerviosas y empeorando la condición de enfermedades como el Alzheimer o la esclerosis lateral amiotrófica (ELA). En otras palabras, la gliosis puede ser tanto protectora como perjudicial, dependiendo de cómo se regule.
En la revisión de 2024, los investigadores profundizan en cómo la vía PI3K/AKT, una ruta de señalización molecular, regula varios aspectos del comportamiento de los astrocitos durante este proceso. Esta vía tiene un impacto directo en la migración de los astrocitos hacia las áreas dañadas, en la formación de cicatrices gliales que protegen el cerebro, y en la inflamación que se desencadena como parte de la respuesta protectora. Sin embargo, cuando la vía PI3K/AKT se activa de manera descontrolada, puede inducir una inflamación excesiva y prolongada, lo que contribuye al daño neuronal crónico.
El hallazgo más relevante de la revisión es la identificación de una alteración en la activación de esta vía en los astrocitos reactivos, es decir, aquellos que responden a las lesiones cerebrales. Este descubrimiento se basa en el análisis de datos bioinformáticos, que mostraron una mayor expresión de genes relacionados con la vía PI3K/AKT en los astrocitos reactivos en comparación con los astrocitos normales. Además, se encontró que los niveles de las proteínas clave en esta vía, como PI3K y AKT, estaban elevados en astrocitos de ratones, tanto en aquellos derivados de modelos normales como los con la mutación genética asociada a la ELA.
Otro hallazgo crucial, es el papel de la proteína Connexin43 (Cx43), que es un componente esencial en la comunicación entre células del cerebro. Durante la gliosis, esta proteína se fosforila —un proceso químico que la activa—, lo que permite la apertura de un canal en la membrana de los astrocitos. Este canal abierto lleva a la liberación de ATP, una molécula que no solo sirve como fuente de energía, sino que también actúa como una señal en la inflamación del cerebro. La liberación de ATP juega un papel fundamental en la astrogliosis, ya que ayuda a coordinar la respuesta inflamatoria y facilita la migración de los astrocitos hacia las áreas dañadas. Sin embargo, si este proceso se activa en exceso, puede contribuir a la inflamación crónica y al daño neuronal.
Los astrocitos son importantes en el respaldo de las funciones neuronales, pero en un cerebro sano nunca se mueven. Sin embargo, cuando los astrocitos son sometidos a procesos inflamatorios, cambian de forma y comienzan a migrar. En el artículo de Leyton y colaboradores, la vía de señalización molecular que se activa en los astrocitos migratorios pudo ser mitigada en un modelo preclínico usando un inhibidor de AKT, el que disminuyó el daño neuronal causado por la inflamación.
Los investigadores sugieren entonces que la vía PI3K/AKT es un objetivo terapéutico prometedor para controlar la reactividad de los astrocitos y así disminuir los efectos negativos de la gliosis. Modificar esta vía podría ser una forma de reducir la inflamación excesiva sin interferir con los mecanismos protectores de los astrocitos, lo que ofrecería nuevas oportunidades para tratar enfermedades neurodegenerativas como la ELA y el Alzheimer. Según Lisette Leyton, autora principal del estudio, “El control de la activación de la vía PI3K/AKT podría permitirnos tratar de manera más efectiva las enfermedades inflamatorias del cerebro, modulando la respuesta de los astrocitos de forma precisa y reduciendo el daño a largo plazo”.
En conclusión, la revisión publicada en 2024, junto con los hallazgos previos de 2023, subraya la importancia de comprender los mecanismos subyacentes a la gliosis y su potencial para desarrollar nuevas estrategias terapéuticas. Los avances en este campo podrían ser fundamentales para el desarrollo de tratamientos más específicos y efectivos que aborden las causas subyacentes de las enfermedades neurodegenerativas y mejoren la calidad de vida de los pacientes.
Leer nota completa en Ciencia En Chile